এই সমাধান গাইড সম্পর্কে
মাধ্যমিক ২০১৭ সালের ভৌতবিজ্ঞান প্রশ্নপত্রের সম্পূর্ণ সমাধান গাইডে আপনাকে আন্তরিক স্বাগতম! 🌟
এই রিসোর্সটি বিশেষভাবে শ্রেণি ১০-এর ছাত্রছাত্রীদের জন্য তৈরি, যাতে তারা শুধু উত্তর মুখস্থ না করে, প্রতিটি বিষয়ের মূল ধারণা গভীরভাবে বুঝতে পারে।
এখানে প্রতিটি প্রশ্নের সাথে রয়েছে সহজবোধ্য ও বিশদ ব্যাখ্যা, যা আপনাকে বিষয়টির অন্তর্নিহিত নীতি ও প্রয়োগ বোঝাতে সহায়তা করবে। আপনি যদি পরীক্ষার প্রস্তুতি নিচ্ছেন বা পুনরাভ্যাস (রিভিশন) করছেন — এই গাইডটি হবে আপনার একান্ত সহায়ক সঙ্গী। 🔬📘
চলুন, একসাথে বিজ্ঞানের জগতে আরও এক ধাপ এগিয়ে যাই! 🚀
প্রধান বৈশিষ্ট্যসমূহ
- মাধ্যমিক ২০১৭ সালের সম্পূর্ণ প্রশ্নপত্রের বিশদ সমাধান
- প্রতিটি প্রশ্নের জন্য ধাপে ধাপে পরিষ্কার ব্যাখ্যা
- মূল ধারণা ও সূত্রগুলির সহজবোধ্য বিশ্লেষণ
- সহজ নেভিগেশনের জন্য ইন্টারেক্টিভ প্রশ্ন তালিকা
- মোবাইল ও ডেস্কটপ উভয় ডিভাইসের জন্য সম্পূর্ণ উপযোগী ডিজাইন
📝 পরীক্ষার প্রস্তুতির টিপস
শুধু উত্তর মুখস্থ না করে, প্রতিটি বিষয়ের ধারণা গভীরভাবে বোঝার চেষ্টা করুন। এতে আপনি এমন প্রশ্নেরও সঠিক উত্তর দিতে পারবেন, যেগুলি পরীক্ষায় অন্যভাবে উপস্থাপিত হলেও মূলত একই ধারণার উপর ভিত্তি করে তৈরি। মনে রাখবেন — বোঝা শেখা মুখস্থ করার চেয়ে অনেক বেশি শক্তিশালী। 💡
বিভাগ-ক: বহু বিকল্পভিত্তিক প্রশ্ন
(a) মিথেন
(b) জলীয় বাষ্প
(c) কার্বন ডাইঅক্সাইড
(d) অক্সিজেন
মিথেন, জলীয় বাষ্প ও কার্বন ডাইঅক্সাইড গ্রীনহাউস গ্যাস হলেও অক্সিজেন নয়, কারণ এটি ইনফ্রারেড বিকিরণ কার্যকরভাবে শোষণ করে না।
(a) Nm\(^2\)
(b) Nm\(^{-2}\)
(c) Nm
(d) N
তাই চাপের SI একক হবে \( \mathrm{N/m^2} \) বা \( \mathrm{Nm^{-2}} \), যা ‘পাস্কাল’ (\( \text{Pa} \)) নামে পরিচিত।
(a) 8
(b) 16
(c) 32
(d) 64
আণবিক ওজন = 2 × বাষ্পঘনত্ব।
সুতরাং, আণবিক ওজন = 2 × 32 = 64।
(a) উষ্ণতা
(b) দৈর্ঘ্য
(c) উপাদানের প্রকৃতি
(d) প্রস্তুচ্ছেদ
এটি বস্তুটির দৈর্ঘ্য বা প্রস্তুচ্ছেদের উপর নির্ভর করে না।
a. f=2r
b. f=r/2
c. f=r/3
d. f=(2/3) r
অর্থাৎ, \( f = \dfrac{r}{2} \)।
(a) লাল
(b) হলুদ
(c) বেগুনি
(d) সবুজ
তাই এটি প্রিজমের মধ্য দিয়ে যাওয়ার সময় সবচেয়ে বেশি বিচ্যুত হয়।
(a) কুলম্ব.সেকেন্ড
(b) ভোল্ট, ওহম\(^{-1}\)
(c) ভোল্ট.ওহম
(d) ভোল্ট\(^2\)-ওহম
তাই \( I = \dfrac{V}{R} = V \cdot \Omega^{-1} \)।
অতএব, অ্যাম্পিয়ারকে ভোল্ট-ওহম\(^{-1}\) হিসাবে প্রকাশ করা যায়।
(a) পরিবাহী
(b) অর্ধপরিবাহী
(c) অতি পরিবাহী
(d) অন্তরক
ফলে পরিবাহিতা বৃদ্ধি পায় এবং রোধাঙ্ক হ্রাস পায়।
(a) \( \alpha > \beta > \gamma \)
(b) \( \alpha > \gamma > \beta \)
(c) \( \gamma > \beta > \alpha \)
(d) \( \beta > \alpha > \gamma \)
এরপর বিটা কণার, আর গামা রশ্মির আয়নায়ন ক্ষমতা সবচেয়ে কম।
(a) K
(b) H
(c) Li
(d) Na
কারণ পর্যায় সারণীতে একটি গ্রুপে নিচের দিকে নামলে পরমাণুর আকার বৃদ্ধি পায়,
এবং K গ্রুপ ১-এর Na ও Li-এর নিচে অবস্থিত।
(a) হাইড্রোজেন ক্লোরাইড
(b) সোডিয়াম ক্লোরাইড
(c) লিথিয়াম হাইড্রাইড
(d) ক্যালশিয়াম অক্সাইড
যেখানে ইলেকট্রন হাইড্রোজেন ও ক্লোরিন পরমাণুর মধ্যে ভাগ করা হয়।
অন্যান্য যৌগগুলি আয়নিক প্রকৃতির।
(a) CH\(_3\)COOH
(b) NaOH
(c) H\(_2\)SO\(_4\)
(d) NaCl
কারণ এটি জলীয় দ্রবণে আংশিকভাবে আয়নিত হয়।
অন্যগুলি শক্তিশালী তড়িৎবিশ্লেষ্য যা সম্পূর্ণরূপে বিচ্ছিন্ন হয়।
(a) গাঢ় H\(_2\)SO\(_4\)
(b) P\(_2\)O\(_5\)
(c) CaO
(d) CaCl\(_2\)
কারণ এটি অ্যামোনিয়ার সাথে বিক্রিয়া করে না।
গাঢ় H\(_2\)SO\(_4\) অ্যামোনিয়ার সাথে বিক্রিয়া করে,
এবং P\(_2\)O\(_5\) কেবল জল শোষণকারী পদার্থ।
(a) বক্সাইট
(b) হেমাটাইট
(c) ম্যালাকাইট
(d) চ্যালকোপাইরাইটস
হেমাটাইট লোহার আকরিক,
ম্যালাকাইট তামার আকরিক,
এবং চ্যালকোপাইরাইটসও তামার আকরিক।
a. -OH
b. -CHO
c. -COOH
d. >CO
-OH অ্যালকোহলের জন্য,
-COOH কার্বক্সিলিক অ্যাসিডের জন্য,
এবং >CO কিটোনের জন্য।
বিভাগ-খ: সংক্ষিপ্ত উত্তরধর্মী প্রশ্ন
গড়ে প্রতি কিলোমিটারে প্রায় 6.5°C করে তাপমাত্রা কমে।
ফলে সমুদ্রপৃষ্ঠের উচ্চতা বৃদ্ধি পায় এবং উপকূলীয় অঞ্চলে প্লাবনের ঝুঁকি বেড়ে যায়।
এই ক্লোরিন পরমাণু অনুঘটকের মতো কাজ করে ওজন (O\(_3\))-কে অক্সিজেন (O\(_2\))-এ বিভাজিত করে,
ফলে ওজন স্তর ক্ষয় ঘটে।
একই তাপমাত্রা ও চাপে সমআয়তন সমস্ত গ্যাসে অণুর সংখ্যা সমান থাকে।
তাই CO₂ ও N₂-এ অণুর সংখ্যা সমান।
স্থির তাপমাত্রায় একটি নির্দিষ্ট পরিমাণ গ্যাসের জন্য চাপ (P) আয়তনের (V) ব্যস্তানুপাতিক।
গাণিতিকভাবে, \( P \propto \dfrac{1}{V} \) বা \( PV = \text{constant} \)।
এটি তরলের প্রকৃত প্রসারণ নির্দেশ করে,
যা পাত্রের প্রভাবে পরিবর্তিত হয় না।
এটি নির্দেশ করে একক দৈর্ঘ্যে একক তাপমাত্রা পার্থক্যে কত তাপ সঞ্চালিত হয়।
এটি ঘটে যখন সূর্যালোক বায়ুমণ্ডলের জলকণার দ্বারা প্রতিসৃত, প্রতিফলিত ও বিচ্ছুরিত হয়,
যার ফলে সাদা আলো তার উপাদান রঙগুলোতে বিভক্ত হয়ে যায়।
এই লেন্স আলোকে চোখে প্রবেশের আগে অপসারিত করে,
ফলে চিত্রটি রেটিনায় সঠিকভাবে ফোকাস করতে পারে।
যখন তড়িৎপ্রবাহের দিক উল্টে যায়, তখন ফ্লেমিংয়ের বাম হাতের নিয়ম অনুসারে চৌম্বক বলের দিকও উল্টে যায়,
ফলে চাকাটির ঘূর্ণনের দিকও বিপরীত হয়।
সুতরাং, \( W = 1\,C \times 1\,V = 1\,J \)।
অর্থাৎ 1 কুলম্ব আধান স্থানান্তর করতে 1 জুল কার্য করতে হবে।
যখন একটি নিউট্রন প্রোটনে রূপান্তরিত হয় এবং একটি ইলেকট্রন ও অ্যান্টিনিউট্রিনো নির্গত হয়।
\( ^{238}_{92} \text{U} \rightarrow ^{234}_{90} \text{Th} + ^4_2\alpha \)
তাই উৎপন্ন মৌল থোরিয়ামের পারমাণবিক সংখ্যা 90।
| বাম স্তম্ভ | ডান স্তম্ভ |
| 2.11.1 একটি সন্ধিগত মৌল | (a) অ্যালুমিনিয়াম |
| 2.11.2 একটি ইউরেনিয়ামোত্তর মৌল | (b) নিকেল |
| 2.11.3 থার্মিট পদ্ধতিতে উচ্চ উষ্ণতায় Fe₂O₃ কে বিজারিত করে | (c) টিন |
| 2.11.4 ধাতুর সংকর কাঁসাতে উপস্থিত | (d) প্লুটোনিয়াম |
| বাম স্তম্ভ | ডান স্তম্ভ |
| 2.11.1 একটি সন্ধিগত মৌল | (b) নিকেল |
| 2.11.2 একটি ইউরেনিয়ামোত্তর মৌল | (d) প্লুটোনিয়াম |
| 2.11.3 থার্মিট পদ্ধতিতে উচ্চ উষ্ণতায় Fe₂O₃ কে বিজারিত করে | (a) অ্যালুমিনিয়াম |
| 2.11.4 ধাতুর সংকর কাঁসাতে উপস্থিত | (c) টিন |
ব্যাখ্যা:
• নিকেল একটি সন্ধিগত (transition) মৌল (d-ব্লক)।
• প্লুটোনিয়াম ইউরেনিয়ামোত্তর (actinide/ transuranic) মৌল — পারমাণবিক সংখ্যা ৯২-এর উপরে।
• থার্মিট পদ্ধতিতে অ্যালুমিনিয়াম লোহা (Fe₂O₃) থেকে লৌহ (Fe) বিজারিত করে: \(2\text{Al} + \text{Fe}_2\text{O}_3 \rightarrow 2\text{Fe} + \text{Al}_2\text{O}_3\)。
• কাঁসা হলো তামা (Cu) ও টিন (Sn) এর সংকর ধাতু।
ফ্লোরিন পরমাণু (পারমাণবিক সংখ্যা 9) এর ইলেকট্রন বিন্যাস: 2,7।
প্রতিটি ফ্লোরিনকে অষ্টক পূর্ণ করতে একটি ইলেকট্রন দরকার।
F₂ অণুতে দুটি ফ্লোরিন পরমাণু একটি জোড়া ইলেকট্রন ভাগ করে (একটি একক বন্ধন)।
লুইস গঠন: :F ─ F: । প্রতিটি ফ্লোরিন পরমাণুর ৩টি একাকী জোড় (৬টি ইলেকট্রন) এবং ১টি ভাগ করা জোড় (২টি ইলেকট্রন) থাকে।
বিশুদ্ধ জলের নিজস্ব আয়ন সংখ্যা অত্যন্ত কম, তাই তার বৈদ্যুতিক পরিবাহিতা কম।
সালফিউরিক অ্যাসিড (H₂SO₄) জলীয় দ্রবণে আয়নিত হয়ে H⁺ ও SO₄²⁻ প্রদান করে, যা আধান বাহক হিসেবে কাজ করে—পরিবাহিতা বাড়ে।
তড়িৎ বিশ্লেষণের সময় বিদ্যুত পরিবহণ করে আয়নগুলো — ক্যাটায়ন (ধনাত্মক) ক্যাথোডের দিকে এবং অ্যানায়ন (ঋণাত্মক) অ্যানোডের দিকে ধাবিত হয়।
CuSO₄ দ্রবণে ক্যাটায়ন হল Cu\(^{2+}\), যা ক্যাথোডের দিকে চলে।
ক্যাথোডে: Cu\(^{2+}\) + 2e\(^{-}\) → Cu (তামার নিক্ষেপণ)।
অ্যানোডে: Cu → Cu\(^{2+}\) + 2e\(^{-}\) (তামা দ্রবীভূত হয়) এবং SO₄\(^{2-}\) অ্যানোডের দিকে থাকে।
Pb(NO₃)₂ + H₂S → PbS ↓ + 2HNO₃।
লেড সালফাইড (PbS) একটি কালো অধঃক্ষেপ, তাই কালো পত্রিকা PbS দ্বারা সৃষ্টি হয়।
H₂S চালনার ফলে ডাইক্রোমেট (Cr₂O₇²⁻) কমলা রঙ হ্রাস পেয়ে ক্রোমিয়াম(III) (Cr³⁺) এর সবুজ রঙে পরিবর্তিত হয়।
রসায়নাত্মক প্রতিক্রিয়া (উদাহরণ):
K₂Cr₂O₇ + 4H₂SO₄ + 3H₂S → K₂SO₄ + Cr₂(SO₄)₃ + 7H₂O + 3S
প্রতিক্রিয়া: 2NH\(_3\) + CO\(_2\) → NH\(_2\)CONH\(_2\) + H\(_2\)O।
এই প্রক্রিয়াটি সাধারণত উচ্চ চাপ (150–250 atm) ও উচ্চ তাপমাত্রায় (180–200°C) সম্পন্ন করা হয়।
• জল পাইপ এবং প্লাম্বিং ফিটিং
• বৈদ্যুতিক কেবলের নিরোধক
• ফ্লোরিং উপকরণ ও উইন্ডো ফ্রেম
• কিছু চিকিৎসা যন্ত্রপাতি ও প্যাকেজিং উপকরণেও ব্যবহৃত হয়।
উভয়ের অণুঘনতা একই (C\(_2\)H\(_6\)O) কিন্তু কার্যকরী গ্রুপ ভিন্ন (অ্যালকোহল বনাম ইথার)।
বিভাগ-গ: সংক্ষিপ্ত উত্তরধর্মী প্রশ্ন
এটি সাধারণত কিলোজুল প্রতি কিলোগ্রাম (kJ/kg)-এ প্রকাশ করা হয়।
কয়লার তুলনায় ডিজেলের তাপনমূল্য বেশি — প্রায় 45,500 kJ/kg, যেখানে কয়লার তাপনমূল্য প্রায় 25,000–33,000 kJ/kg।
বয়েলের সূত্র অনুযায়ী, \( P_1V_1 = P_2V_2 \)
STP-তে, \( P_1 = 76 \, cmHg \), \( V_1 = 52 \, m^3 \)
নতুন চাপে, \( P_2 = 104 \, cmHg \)
তাই \( V_2 = \frac{P_1V_1}{P_2} = \frac{76 \times 52}{104} = 38 \, m^3 \)
আদর্শ গ্যাস সমীকরণ ব্যবহার করে: \( PV = nRT \)
H₂-এর মোলার ভর = 2 g/mol
মোল সংখ্যা, \( n = \frac{8}{2} = 4 \, mol \)
\( V = \frac{nRT}{P} = \frac{4 \times 0.082 \times 300}{4} = 24.6 \, L \)
\( \mu = \frac{c}{v} \), যেখানে c = শূন্যস্থানে আলোর বেগ এবং v = মাধ্যমের মধ্যে আলোর বেগ।
সুতরাং, কোনো মাধ্যমের আলোর বেগ যত কম, প্রতিসরাঙ্ক তত বেশি।
আলোর উৎস ফোকাসে রাখলে, প্রতিফলনের ফলে দর্পণ থেকে শক্তিশালী সমান্তরাল আলোর রশ্মি বের হয়,
যা দূর পর্যন্ত আলোকিত করে।
১. উচ্চ দক্ষতা: CFL বিদ্যুৎ শক্তির প্রায় ২০–২৫% দৃশ্যমান আলোতে রূপান্তর করে, যেখানে ভাস্বর বাল্ব মাত্র ৫% করে।
২. দীর্ঘ জীবনকাল: CFL ভাস্বর বাল্বের তুলনায় ৮–১৫ গুণ বেশি স্থায়ী (প্রায় ৮০০০ ঘন্টা বনাম ১০০০ ঘন্টা)।
অতিরিক্ত সুবিধা: কম তাপ উৎপন্ন হয়, শক্তি সঞ্চয় হয়, ফলে দীর্ঘমেয়াদে অর্থনৈতিক।
চিনি (C₁₂H₂₂O₁₁) একটি সমযোজী যৌগ যা জলে আয়নিত হয় না,
তাই এটি বৈদ্যুতিক পরিবাহিতা প্রদর্শন করতে পারে না।
অন্যদিকে, সোডিয়াম ক্লোরাইড (NaCl) একটি আয়নিক যৌগ যা জলে Na⁺ ও Cl⁻ আয়নে বিভক্ত হয়,
ফলে দ্রবণটি তড়িৎ পরিবাহিতা প্রদর্শন করে।
এটি আয়ন-স্ট্রাকচারে (স্ফটিক জালকে) উপস্থিত থাকে, তাই একক সূত্র (NaCl)-এর ভর উল্লেখ করতে "সাংকেতিক ওজন" (formula mass) শব্দটি বেশি সঙ্গতিপূর্ণ—"আণবিক ওজন" (molecular mass) ব্যবহৃত হয় এমন কেবল অণুগুলোর জন্য।
গলনাঙ্ক: সোডিয়াম ক্লোরাইডের শক্তিশালী আয়নিক বন্ধনের কারণে এর গলনাঙ্ক উচ্চ (প্রায় 801°C)।
ন্যাপথলিনের মধ্যে শুধুমাত্র দুর্বল আন্তঃআণবিক শক্তি (ভ্যান ডার ভ্যালস) কাজ করে, তাই এর গলনাঙ্ক তুলনামূলকভাবে অনেক কম (প্রায় 80°C)।
জলে দ্রাব্যতা: NaCl আয়ন-ডাইপোল ইন্টারঅ্যাকশনের ফলে জলে ভালভাবে দ্রবণীয়;
ন্যাপথলিন অ-মেরুীয় এবং জলের সঙ্গে শক্তিশালী হাইড্রোজেন/ডাইপোল ইন্টারঅ্যাকশন করতে না পারায় জলে অদ্রবণীয়।
দ্বিতীয় অংশ (প্রস্তুতি):
কিপের যন্ত্রে সাধারণত একটি সলিড সালফাইডের উপর অম্ল প্রয়োগ করে H₂S প্রস্তুত করা হয়। উদাহরণস্বরূপ:
\( \text{FeS} + 2\text{HCl} \rightarrow \text{FeCl}_2 + \text{H}_2\text{S} \uparrow \)
দ্রষ্টব্য:কিপ যন্ত্রে CO₂ (CaCO₃ + 2HCl → CaCl₂ + CO₂ ↑) বা H₂ (Zn + 2HCl → ZnCl₂ + H₂ ↑) ইত্যাদিও প্রস্তুত করা যায়।
\( 2\text{ZnO} + \text{C} \rightarrow 2\text{Zn} + \text{CO}_2 \)
এখানে কার্বন অক্সাইড (CO₂) সৃষ্টি হয় এবং ZnO থেকে Zn বিজারিত হয়।
\( \text{Zn} + \text{CuSO}_4 \rightarrow \text{ZnSO}_4 + \text{Cu} \)
ইলেকট্রনীয় তত্ত্ব অনুযায়ী (রেডক্স বিবরণ):
• জিংক অটোম দুই ইলেকট্রন হারায়: \( \text{Zn} \rightarrow \text{Zn}^{2+} + 2e^- \) (জারণ)
• তামা আয়ন দুই ইলেকট্রন গ্রহন করে: \( \text{Cu}^{2+} + 2e^- \rightarrow \text{Cu} \) (বিজারণ)
ফলে এটি একটি রেডକস (জারণ-বিজারণ) বিক্রিয়া।
H₂C=CH₂
এখানে কার্বন-কার্বন দ্বি-বন্ধনের (C=C) উপস্থিতি ইথিলিনকে অসম্পৃক্ত হাইড্রোকার্বন হিসাবে পরিচিত করে।
অসম্পৃক্ত যৌগ সাধারণত সংযোজন বিক্রিয়া করতে সক্ষম।
এটি শিল্পে দ্রাবক ও জ্বালানী হিসেবে ব্যবহৃত হয় এবং ভোক্যা-পানীয় হিসেবে ব্যবহার অনুপযোগী করা হয়।
বিভাগ-ঘ: দীর্ঘ উত্তরধর্মী প্রশ্ন
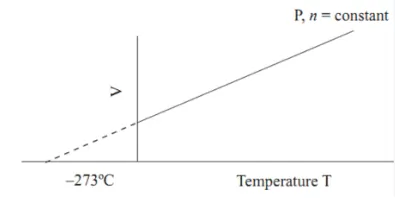
চার্লসের সূত্র: স্থির চাপে, একটি নির্দিষ্ট ভরের গ্যাসের আয়তন তার পরম তাপমাত্রার সাথে সরাসরি সমানুপাতিক।
গাণিতিকভাবে: \( V \propto T \) বা \( \frac{V}{T} = \text{ধ্রুবক} \)
গ্রাফিকাল উপস্থাপনা:
বিক্রিয়া: \( (\text{NH}_4)_2\text{SO}_4 + 2\text{NaOH} \rightarrow \text{Na}_2\text{SO}_4 + 2\text{NH}_3 + 2\text{H}_2\text{O} \)
NH₃-এর মোলার ভর = 14 + 1×3 = 17 g/mol
(NH₄)₂SO₄-এর মোলার ভর = (14 + 1×4)×2 + 32 + 4×16 = 132 g/mol
সমীকরণ থেকে: 2 মোল NH₃ (34g) থেকে 1 মোল (NH₄)₂SO₄ (132g)
6.8g NH₃-এর জন্য, প্রয়োজনীয় (NH₄)₂SO₄ = \( \frac{132}{34} \times 6.8 = 26.4 \) g
বিক্রিয়া: \( \text{CaCO}_3 + 2\text{HCl} \rightarrow \text{CaCl}_2 + \text{CO}_2 + \text{H}_2\text{O} \)
HCl-এর মোলার ভর = (1 + 35.5) g/mol = 36.5 g/mol
উপরের রাসায়নিক বিক্রিয়া থেকে বোঝা যাচ্ছে যে, 1 মোল CaCO₃ \((=40+12+3 \times 16 =100g)\) 2 মোল HCl \((2\times 36.5 = 73g)\) প্রয়োজন
50g CaCO₃-এর জন্য, প্রয়োজনীয় HCl = \( \frac{73}{100} \times 50 = 36.5 \) g
কিন্তু আমাদের নির্দিষ্ট পরিমাণ উৎপাদন করতে হবে:
55.5g CaCl₂ (0.5 মোল) থেকে, আমাদের 1 মোল HCl = 36.5g প্রয়োজন
22.2g CO₂ (0.5 মোল) থেকে, আমাদের 1 মোল HCl = 36.5g প্রয়োজন
9.0g H₂O (0.5 মোল) থেকে, আমাদের 1 মোল HCl = 36.5g প্রয়োজন
মোট HCl প্রয়োজন = 36.5g
HCl-এর মোল = \( \frac{36.5}{36.5} = 1 \) মোল
1. উভয়ই একই রকম গাণিতিক সমীকরণ অনুসরণ করে (তাপের জন্য ফুরিয়ারের সূত্র, বিদ্যুতের জন্য ওহমের সূত্র)
2. উভয়ই উপাদানের বৈশিষ্ট্যের উপর নির্ভর করে (তাপ পরিবাহিতা এবং বৈদ্যুতিক পরিবাহিতা)
উচ্চ তাপ পরিবাহিতা সহ অধাতু: হীরার অ-ধাতুগুলির মধ্যে সর্বোচ্চ তাপ পরিবাহিতা রয়েছে (তামার প্রায় 5 গুণ)।
প্রতিসরণের দ্বিতীয় সূত্র (স্নেলের সূত্র): আপতন কোণের sine এবং প্রতিসরণ কোণের sine-এর অনুপাত একটি নির্দিষ্ট জোড়া মাধ্যমের জন্য ধ্রুবক।
গাণিতিক সূত্র: \( \frac{\sin i}{\sin r}\) = ধ্রুবক = \(\mu \)
যেখানে \( \mu \) হল প্রথম মাধ্যমের সাপেক্ষে দ্বিতীয় মাধ্যমের প্রতিসরাঙ্ক।
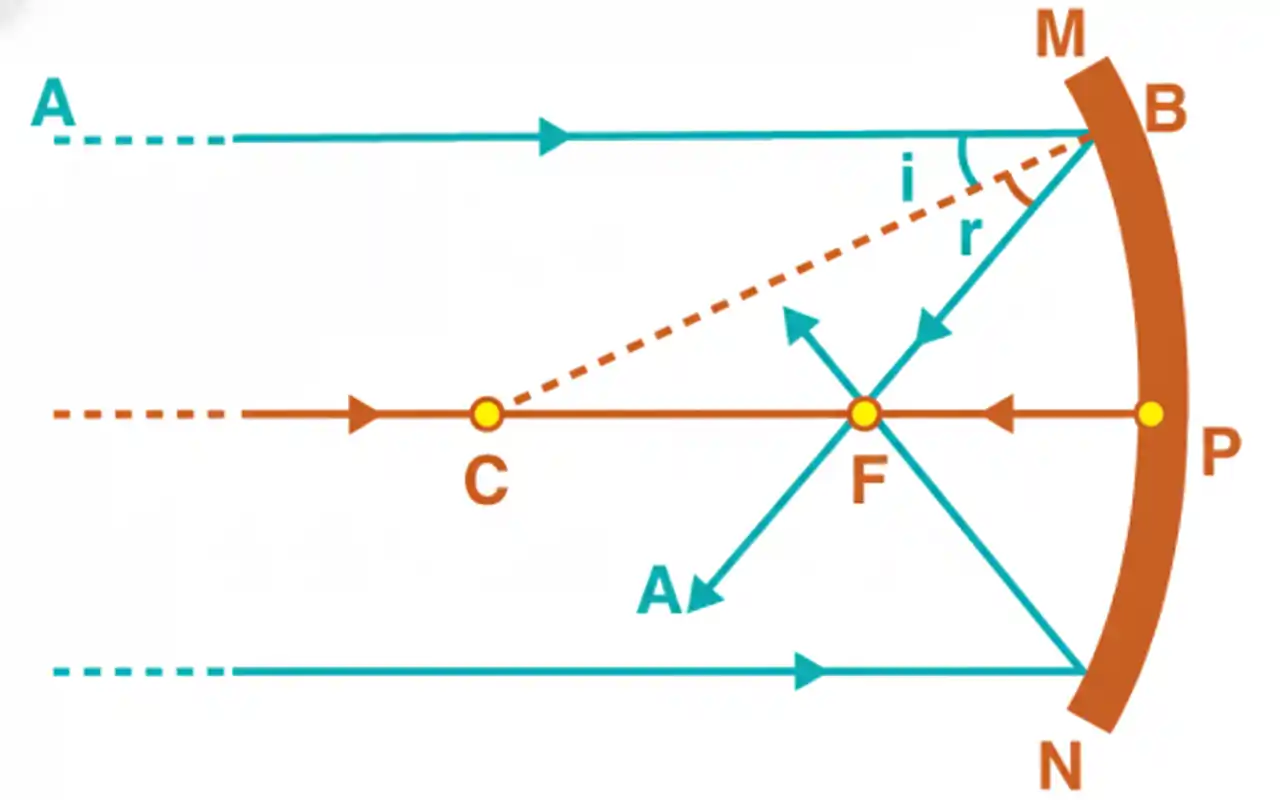
একটি আলোক রশ্মি AB মুখ্য অক্ষের সমান্তরাল হয়ে গোলাকার দর্পণের B বিন্দুতে আপতিত হয়। B বিন্দুতে পৃষ্ঠের অভিলম্ব হিসাবে কাজ করে CB। বক্রতা ব্যাসার্ধ CP = CB = R হিসাবে চিহ্নিত। আলো দর্পণ থেকে প্রতিফলিত হওয়ার পর, এটি অবতল দর্পণের ফোকাস F-এ মিলিত হয়, প্রতিফলনের সূত্র মেনে চলে, যা বলে যে আপতন কোণ প্রতিফলন কোণের সমান (i = r)।
চিত্রের জ্যামিতি থেকে,
∠BCP = θ = i (যেহেতু ∠BCP এবং ∠ABC একান্তর কোণ)
ΔCBF-এ, ∠CBF = θ = r
∴ BF = FC (কারণ i = r)
যদি দর্পণের রন্ধ্র ছোট হয়, B P-এর কাছাকাছি অবস্থিত, এবং তাই BF = PF
=> FC = BF = PF
=> PC = PF + FC = PF + PF
=> R = 2 PF = 2f
=> f = R/2 (প্রমাণিত)
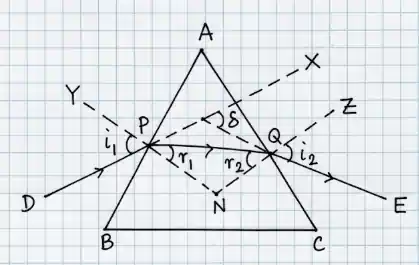
চতুর্ভুজ APNQ-তে: \( \angle A + \angle PNQ = 180^\circ \) ...(1)
ত্রিভুজ PNQ-তে: \( r_1 + r_2 + \angle PNQ = 180^\circ \) ...(2)
(1) এবং (2) থেকে: \( A = r_1 + r_2 \)
বিচ্যুতি কোণ: \( \delta = (i_1 - r_1) + (i_2 - r_2) \)
\( \delta = i_1 + i_2 - (r_1 + r_2) \)
\( \delta = i_1 + i_2 - A \)
ফ্যারাডের দ্বিতীয় সূত্র: আবিষ্ট emf-এর মাত্রা বন্ধ কুণ্ডলীর সাথে যুক্ত চৌম্বক ফ্লাক্সের পরিবর্তনের হারের সরাসরি সমানুপাতিক।
গাণিতিকভাবে: \( \epsilon = -N \frac{d\Phi}{dt} \)
যেখানে \( \epsilon \) হল আবিষ্ট emf, N হল পালার সংখ্যা, এবং \( \frac{d\Phi}{dt} \) হল চৌম্বক ফ্লাক্সের পরিবর্তনের হার।
পরিবর্তী প্রবাহ (AC): একটি বৈদ্যুতিক প্রবাহ যা পর্যায়ক্রমে দিক বিপরীত করে এবং সময়ের সাথে ক্রমাগত তার মাত্রা পরিবর্তন করে, একমুখী প্রবাহ (DC) এর বিপরীতে যা শুধুমাত্র এক দিকে প্রবাহিত হয়।
ব্যবহৃত শক্তি = ক্ষমতা × সময় = 0.11 kW × 10 h = 1.1 kWh (BOT একক)
যখন দৈর্ঘ্য দ্বিগুণ হয় (2l), আয়তন স্থির থাকে, তাই ক্ষেত্রফল অর্ধেক হয়ে যায় (A/2)
নতুন রোধ, \( R' = \rho \frac{2l}{A/2} = 4 \times \rho \frac{l}{A} = 4 \times 6 = 24 \) ওহম
নিউক্লিয় সংযোজনে শক্তির উৎস: নিউক্লিয় সংযোজনে, যখন হালকা নিউক্লিয়াস মিলিত হয়ে একটি ভারী নিউক্লিয়াস গঠন করে, তখন উৎপাদ নিউক্লিয়াসের ভর মূল নিউক্লিয়াসের ভরের সমষ্টির চেয়ে কম হয়। আইনস্টাইনের সমীকরণ \( E = \Delta m c^2 \) অনুসারে এই ভর ত্রুটি শক্তিতে রূপান্তরিত হয়, যেখানে \( \Delta m \) হল ভর ত্রুটি এবং c হল আলোর গতি।
উদাহরণ: পারমাণবিক ব্যাসার্ধ একটি পর্যায় জুড়ে (বাম থেকে ডানে) হ্রাস পায় এবং একটি গ্রুপে নিচের দিকে বৃদ্ধি পায়।
অ-পর্যায়ক্রমিক বৈশিষ্ট্য: তেজস্ক্রিয়তা একটি পর্যায়ক্রমিক বৈশিষ্ট্য নয়।
গ্রুপ 1-এ প্রবণতা: গ্রুপ 1-এ (ক্ষার ধাতু) উপর থেকে নিচের দিকে তড়িৎঋণাত্মকতা হ্রাস পায়। এটি কারণ গ্রুপে নিচের দিকে পারমাণবিক আকার বৃদ্ধি পায়, বন্ধন ইলেকট্রন আকর্ষণ করার নিউক্লিয়াসের ক্ষমতা হ্রাস করে।
শক্তির উৎস: তড়িৎ বিশ্লেষণের সময় রাসায়নিক বিক্রিয়ার জন্য বৈদ্যুতিক শক্তি দায়ী। এটি অ-স্বতঃস্ফূর্ত রেডক্স বিক্রিয়া চালানোর জন্য প্রয়োজনীয় শক্তি সরবরাহ করে।
অম্লীয় জলের তড়িৎ বিশ্লেষণ (H₂SO₄-এর কয়েক ফোঁটা সহ জল):
ক্যাথোডে (বিজারণ): \( 2\text{H}^+ + 2e^- \rightarrow \text{H}_2 \uparrow \)
অ্যানোডে (জারণ): \( 2\text{H}_2\text{O} \rightarrow \text{O}_2 \uparrow + 4\text{H}^+ + 4e^- \)
সামগ্রিক বিক্রিয়া: \( 2\text{H}_2\text{O} \rightarrow 2\text{H}_2 \uparrow + \text{O}_2 \uparrow \)
\( 2\text{SO}_2 + \text{O}_2 \xrightarrow[400-450^\circ\text{C}]{\text{V}_2\text{O}_5} 2\text{SO}_3 \)
শর্ত: তাপমাত্রা 400-450°C, চাপ 1.5-1.7 atm, ভ্যানাডিয়াম পেন্টাঅক্সাইড (V₂O₅) অনুঘটক
SO₃ থেকে H₂SO₄ প্রস্তুতি:
SO₃ 98% H₂SO₄-তে দ্রবীভূত হয়ে ওলিয়াম (H₂S₂O₇) গঠন করে:
\( \text{SO}_3 + \text{H}_2\text{SO}_4 \rightarrow \text{H}_2\text{S}_2\text{O}_7 \)
ওলিয়ামকে তখন জল দিয়ে তরল করে ঘন H₂SO₄ পাওয়া যায়:
\( \text{H}_2\text{S}_2\text{O}_7 + \text{H}_2\text{O} \rightarrow 2\text{H}_2\text{SO}_4 \)
\( \text{HC} \equiv \text{CH} + \text{H}_2 \xrightarrow[\text{Ni অনুঘটক}]{200-300^\circ\text{C}} \text{H}_2\text{C} = \text{CH}_2 \) (ইথিন)
\( \text{H}_2\text{C} = \text{CH}_2 + \text{H}_2 \xrightarrow[\text{Ni অনুঘটক}]{200-300^\circ\text{C}} \text{CH}_3 - \text{CH}_3 \) (ইথেন)
LPG-এর ব্যবহার: রান্না এবং গরম করার জন্য গৃহস্থালী জ্বালানী হিসাবে।
\( \text{CH}_3\text{CH}_2\text{OH} \xrightarrow[\text{গাঢ় H}_2\text{SO}_4]{170^\circ\text{C}} \text{CH}_2 = \text{CH}_2 + \text{H}_2\text{O} \)
এটি নिर্জলীকরণ বিক্রিয়া (জল অণু অপসারণ)।
প্রোটিনের বায়োডিগ্রেডেশন: প্রোটিন অণুজীব দ্বারা এনজাইমেটিক হাইড্রোলাইসিসের মাধ্যমে অ্যামিনো অ্যাসিডে ভেঙে যায়, যা আরও সরল যৌগ যেমন CO₂, H₂O এবং NH₃-এ পচে যায়।
বিভাগ-ঙ: বহিরাগত প্রার্থীদের জন্য
তেজস্ক্রিয় রশ্মি: গামা রশ্মি হল তড়িচ্চুম্বকীয় বিকিরণ, কণা নয়। আলফা এবং বিটা রশ্মি কণা নিয়ে গঠিত (হিলিয়াম নিউক্লিয়াস এবং ইলেকট্রন যথাক্রমে)।
CNG উৎস: সংকুচিত প্রাকৃতিক গ্যাস (CNG) প্রাকৃতিক গ্যাস ক্ষেত্র থেকে প্রাপ্ত। এটি প্রাথমিকভাবে মিথেন (CH₄) যা প্রমাণ বায়ুমণ্ডলীয় চাপের 1% এরও কম আয়তনে সংকুচিত।
1. সহজ ভোল্টেজ রূপান্তর: ট্রান্সফরমার ব্যবহার করে AC ভোল্টেজ সহজেই স্টেপ আপ বা স্টেপ ডাউন করা যেতে পারে, দক্ষ দীর্ঘ-দূরত্ব ট্রান্সমিশন সক্ষম করে।
2. কম ট্রান্সমিশন লস: উচ্চ ভোল্টেজে (ট্রান্সমিশনের জন্য ব্যবহৃত), AC-এর DC-এর তুলনায় কম শক্তি ক্ষতি হয়।
অতিরিক্ত সুবিধা: AC মোটর সহজ এবং সস্তা, AC সহজেই উৎপাদন করা যায়।
\( \text{FeCl}_3 + 3\text{NH}_4\text{OH} \rightarrow \text{Fe(OH)}_3 \downarrow + 3\text{NH}_4\text{Cl} \)
লাল-বাদামী অধঃক্ষেপ হল অদ্রবণীয় ফেরিক হাইড্রক্সাইড [Fe(OH)₃]।
\( \text{CH}_4 + 2\text{O}_2 \rightarrow \text{CO}_2 + 2\text{H}_2\text{O} + \text{তাপ} \)
এটি একটি তাপ নির্গমনকারী বিক্রিয়া যা প্রাকৃতিক গ্যাস জ্বালানী হিসাবে ব্যবহৃত হয়।
চূড়ান্ত প্রস্তুতি টিপস
ধারণার স্পষ্টতা
মুখস্থ করার চেয়ে মৌলিক ধারণাগুলি বোঝার উপর ফোকাস করুন।
সময় ব্যবস্থাপনা
গতি বাড়ানোর জন্য বরাদ্দ সময়ের মধ্যে পেপার সমাধান করার অনুশীলন করুন।
রিভিশন
গুরুত্বপূর্ণ সূত্র এবং ধারণাগুলির নিয়মিত সংশোধন অত্যন্ত গুরুত্বপূর্ণ।